Quelles sont les bases de la spectroscopie vibrationnelle ?
Le spectre IR
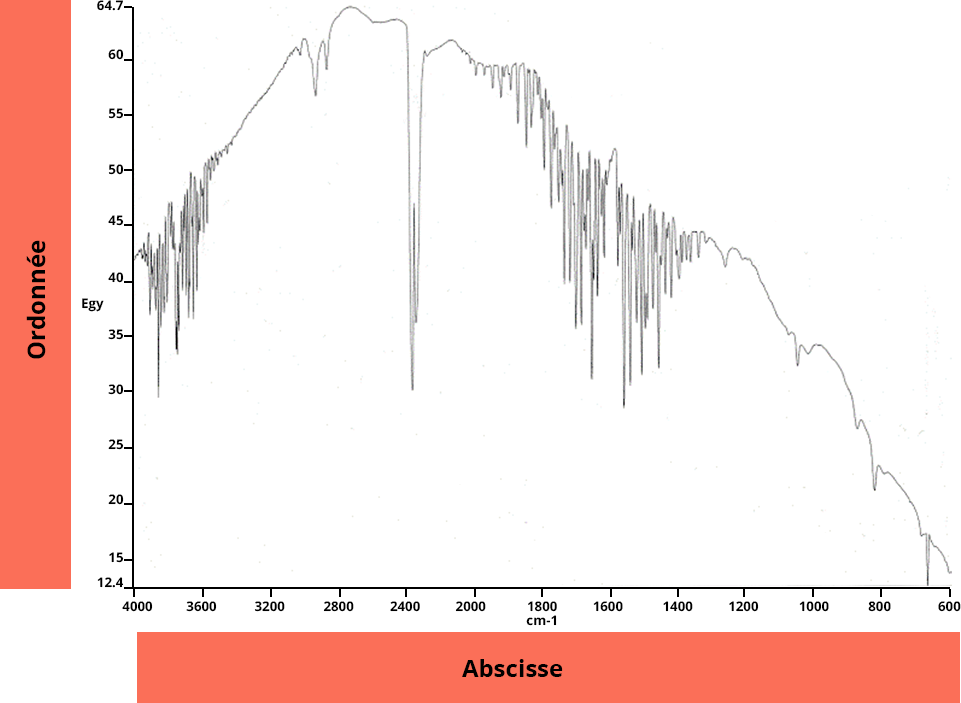
Un spectre IR représente l’intensité d’une radiation IR en fonction du nombre d’onde.
En ordonnée = la transmittance T ou l'absorbance A
T = I/I0 en % avec
I0 = l'intensité lumineuse mesurée sans échantillon (background)
= la contribution de l'appareil + de l'environnement
I = l'intensité lumineuse mesurée en présence d’un échantillon
= la contribution de l'appareil + de l'environnement + de l'échantillon
d'où I/I0 = la contribution de l’échantillon
A = log I0/I sans unité
En abscisse = le nombre d’onde en cm-1
La plupart des molécules organiques vibrent en infra-rouge. Cependant deux conditions sont nécessaires à cela.
Une molécule absorbe la lumière IR si elle possède une vibration pendant laquelle a lieu une variation de son moment dipolaire en fonction de la distance.
Cela se traduit mathématiquement par la relation suivante :

L’énergie de la radiation incidente doit être égale à la différence d’énergie entre deux niveaux vibrationnels de la molécule.

h = 6,63. 10-34 J.S
c = 3 10.10 cm.s-1
ω = nombre d’onde en cm-1