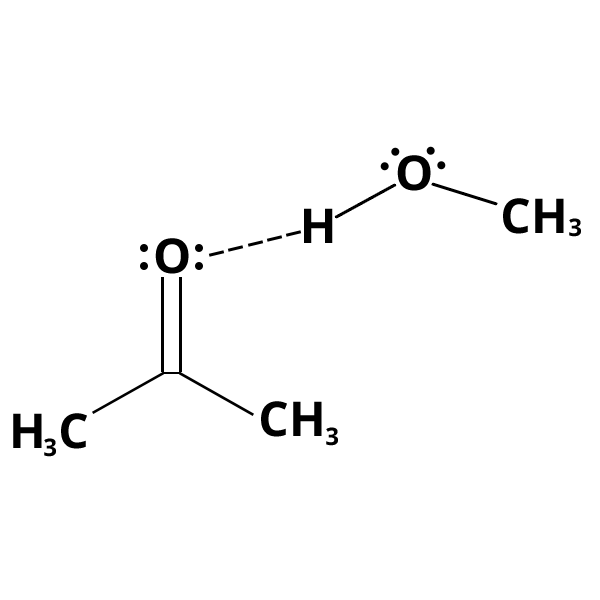
L’interaction de type « liaison hydrogène »
Ces forces particulières se produisent entre les composés possédant des groupes fonctionnels dans lesquels un atome d'hydrogène est lié à un atome électronégatif de petite taille (cf. exemple).
Une liaison hydrogène inter- (ou intra-) moléculaire est formée grâce aux entités X-H et Y :
X-H : ce groupe fournit le proton de la liaison hydrogène (groupe donneur de proton)
Y : groupe donneur d'électrons (présence d'un doublet libre d'électrons).

Cette énergie est de l’ordre de 25 à 40 kJ/mole.