The column: main stage of the retention
La rétention et la séparation des composés en HPLC dépend du couple phase stationnaire (la colonne) et phase mobile (le mélange de solvants). Le mode de chromatographie le plus utilisé actuellement est la chromatographie de partage dit en phase inverse (phase stationnaire apolaire et phase mobile polaire).
La phase stationnaire la plus utilisée en chromatographie de partage dit en phase inverse est composé de silice greffée C18 qui offre de nombreux avantages, mais possède aussi des limites.
La silice greffée C18 : une phase stationnaire quasi universelle…
La silice greffée octadécyle (ou silice greffée C18) est toujours obtenue par un greffage chimique à partir de particules de silice vierges (Si-OH). Les greffons (chaînes alkyles d’octadécane : alcane à 18 carbones - C18) sont fixés de façon covalente sur la silice. Le taux de greffage peut varier selon les fabricants de colonnes. Un traitement de finition (end-capping) est la plupart du temps réalisé pour minimiser les présences de silanols résiduels qui peuvent retenir les composés polaires.
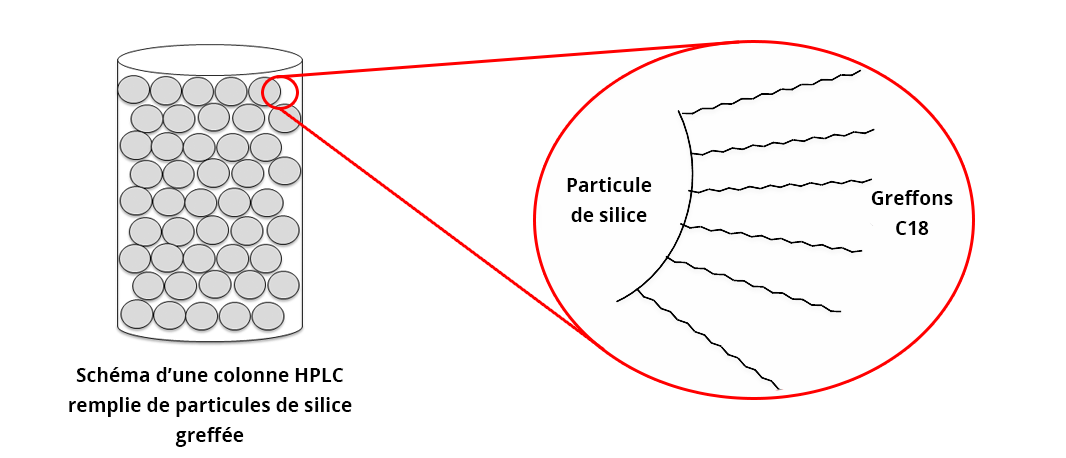
L’octadécane étant un alcane très apolaire, la phase stationnaire de silice greffée C18 aura une très forte affinité avec les composés peu polaires ou apolaires. Pour optimiser la rétention de ces composés, la phase mobile utilisée est souvent aqueuse pour ainsi renforcer les liaisons hydrophobes entre la colonne et les composés d’intérêt (cf. La pompe)
Intérêts et limites de la chromatographie en phase inverse sur colonne C18
| Intérêts | Limites |
|---|---|
| Permet la séparation des composés polaires et apolaires | Mauvaise rétention des composés très polaires |
| Colonne résistante à des conditions extrêmes (pH : 2 – 8 ou 11, utilisation additifs) | Impossible de séparer les isomères |
| Moins de solvant organique utilisé : phase mobile majoritairement aqueuse | Impossible d’utiliser une phase 100 % aqueuse (risque de repli définitif de la structure des greffons C18) |
| Colonne très résistante dans le temps |
La colonne en HPLC
Contrairement aux colonnes de GC, les colonnes utilisées en HPLC ne sont pas creuses, mais remplies de particules de phase stationnaire. Ces particules sont généralement composées de silice qui peuvent ensuite être greffées avec différent groupements polaires ou apolaires (comme la silice greffée C18).
Les colonnes HPLC sont généralement caractérisées par trois grandeurs qui peuvent varier :
- La longueur de la colonne : : varie généralement de 5 cm à 25 cm
- Le diamètre interne : varie généralement entre 4,6 mm et 1 mm
- La taille des particules : varie entre 2 µm et 5 µm (des particules plus fines sont possibles grâce à l’UHPLC)


L’utilisation d’une colonne remplie de particules permet d’améliorer la surface d’échange entre phase mobile et phase stationnaire pour de petites longueurs de colonne. Cependant, la présence de particules de l’ordre du µm engendre de très forte pressions au niveau de l’entrée de la colonne. En HPLC classique, la pression peut atteindre 415 bars, soit une pression équivalente à celle rencontrée au fond des océans. Pour l’UHPLC la pression en tête de colonne peut atteindre 1500 bars, soit une pression plus importante que la pression mesurée dans la faille la plus profonde des océans (12 km de profondeur). A titre de comparaison, la pression des réseaux d’eau courante domestique est de l’ordre de 3 bars.
Le compartiment à colonne thermostaté
Bien que cela puisse paraître anecdotique, posséder un compartiment thermostaté pour la colonne chromatographique joue un rôle important dans la rétention ou l’élution des composés.
En effet, une variation de température dans la colonne pourra modifier le temps de rétention des composés et perturber leur analyse.
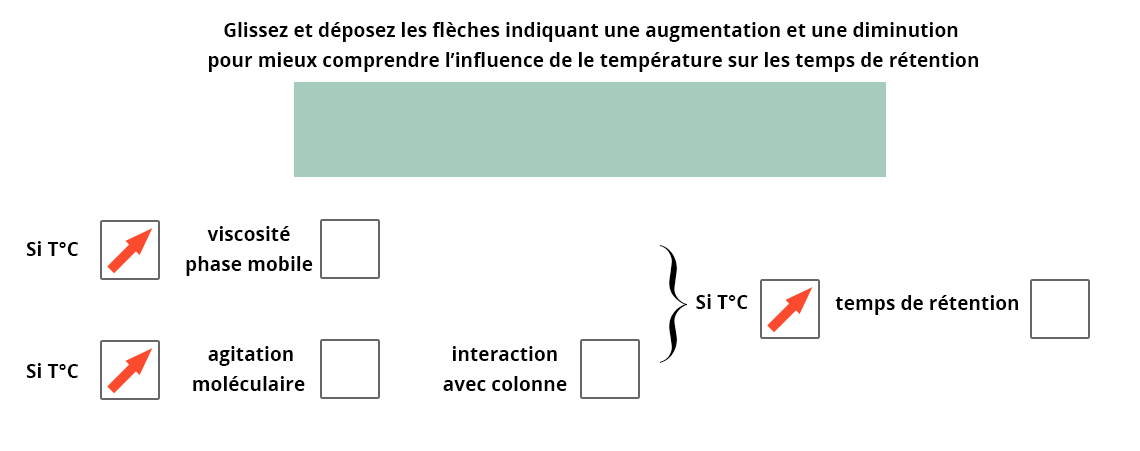




Ne pas thermostater une colonne entrainera une variation des temps de rétention des composés entre hiver et été si la salle n’est pas climatisée.
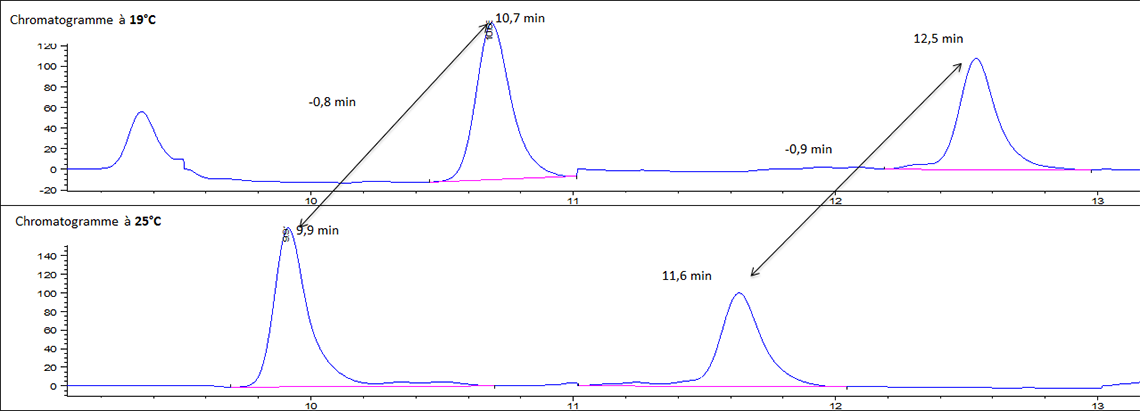
Le chromatogramme ci-dessous, vous permet de constater les différences de rétention des composés analysés entre 19°C (hiver dans une salle chauffée), 25°C (été tempéré). En se basant sur le temps de rétention, il est impossible d’analyser les composés en hiver et en été car ces derniers sont impactés par la température et l’analyse n’est pas reproductible tout au long de l’année
Dans une grande majorité des cas, le compartiment thermostaté (aussi appelé four à colonne) est utilisé pour garantir la stabilité de la température hiver comme été. De ce fait, la température programmée est souvent supérieure à 30°C car les anciens fours ne pouvant réfrigérer, la température doit impérativement être supérieure à une température extérieure en été.
Plus récemment, la technologie des fours à colonne a évolué et ces derniers sont capables de chauffer la colonne ou de la réfrigérer. Cette possibilité a permis de nouvelles applications, notamment en utilisant des séparations à basse température (10°C ou moins) pour maximiser la rétention des composés peu retenus dans la colonne.